Вариант 3. ЧАСТЬ А. Тестовые задания с
выбором ответа
1 (2 балла). Химический элемент, имеющий схему
строения атома 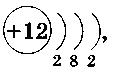 в Периодической системе занимает положение: в Периодической системе занимает положение:
A. 2-й период, главная
подгруппа II группы. Б. 2-й период, главная подгруппа VIII группы.
B. 3-й период, главная подгруппа II группы. Г. 4-й период, главная подгруппа II группы.
2 (2 балла). Строение внешнего энергетического уровня 3s2Sp3 соответствует атому элемента:
А. Алюминия. В. Кремния. , Б. Железа. Г. Фосфора
3. (2 балла). Элемент с
наиболее ярко выраженными неметаллическими свойствами:
А. Германий. В. Олово.
Б. Кремний. Г. Углерод. 4. (2 балла). Оксид элемента Э с зарядом ядра +15 соответствует
общей формуле:
А. ЭО. В. Э2О5. Б. ЭО2. Г. Э2О7.
5 (2 балла). Характер
свойств высшего оксида химического элемента
с порядковым номером 12 в Периодической системе: A. Амфотерный Б. Кислотный. B. Основный.
6 (2 балла). Основные свойства наиболее ярко выражены у гидроксида:
А. Алюминия.
В. Магния. Б. Кремния. Г. Натрия.
 7. (2 балла). Формула вещества,
реагирующего с оксидом углерода (IV): 7. (2 балла). Формула вещества,
реагирующего с оксидом углерода (IV):
A. NaOH. Б. H2SO4. В.
SO3. Г. НС1.
8.(2 балла). Элементом Э в схеме
превращений Э
→ ЭО → Э(ОН)2 является:
А. Алюминий. В. Железо. Б. Барий. Г. Медь.
ЧАСТЬ Б. Задания со свободным ответом
9. (8 баллов). Напишите уравнение реакции между растворами гидроксида элемента с порядковым номером 11 и водородного соединения элемента с порядковым номером 16 в Периодической системе. Назовите все вещества, укажите тип реакции.
10. (8 баллов).По схеме С 1→СО2 2→Na2CO3 3→CaCO3 составьте уравнения
реакций в молекулярном виде. Для превращенияь3
запишите полное и сокращенное ионные уравнения.
Вариант
4 ЧАСТЬ А. Тестовые задания с выбором
ответа
1 (2 балла). Химический элемент,
имеющий схему строения атома 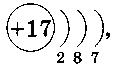 в Периодической системе занимает положение: в Периодической системе занимает положение:
A. 2-й период, главная подгруппа III группы. Б. 2-й период, главная подгруппа VII группы.
B. 3-й период, главная подгруппа V группы. Г. 3-й
период, главная подгруппа VII группы.
2 (2 балла). Строение внешнего энергетического уровня 3s23p6 соответствует
атому элемента:
А. Аргона. В. Никеля. Б. Кислорода. Г. Хлора.
3 (2 балла). Элемент с наиболее ярко выраженными металлическими свойствами:
А. Алюминий. В. Магний. Б. Кремний. Г. Натрий.
4 (2 балла). Оксид элемента Э с зарядом ядра +17 соответствует общей формуле:
А. ЭО. Б. ЭО2. В. Э2О5. Г.Э2О7.
5 (2 балла).
Характер свойств высшего оксида элемента
с порядковым номером 13 в Периодической
системе:
А. Амфотерный. Б.
Кислотный. В. Основный.
6 (2 балла). Кислотные свойства наиболее ярко выражены у высшего гидроксида:
А. Азота. В. Бора. Б. Бериллия. Г.
Углерода.
7. (2 балла). Формула вещества, реагирующего с разбавленной серной кислотой:
А. О2. Б. СаО. В.Сu. Г. СО2.
8. (2 балла). Элементом
Э в схеме превращений Э→ Э2О
→ ЭОН является:
А. Барий. В.
Серебро. Б. Литий. Г.
Углерод.
ЧАСТЬ Б. Задания со свободным ответом
9. (8 баллов). Напишите уравнение реакции между растворами
гидроксида элемента с порядковым номером 19 и
водородного соединения элемента с порядковым номером 35 в Периодической системе. Назовите все вещества, укажите тип
реакции.
10. (6 баллов). По схеме превращений Li 1→Li2O 2→ LiOH 3→ Li2SO4 составьте
уравнения реакций в молекулярном виде. Для
превращения 3 запишите полное и сокращенное ионные
уравнения.
|